Dieser Artikel ist Teil einer Reihe, die die Gründe der NSAID-Intoleranz und des bekanntesten Krankheitsbilds, der Samter Trias, beleuchtet. Der erste Artikel beleuchtet die Störungen im Fettsäurestoffwechsel und die damit eingehende Leukotriene- und Prostaglandinproduktion. Nachfolgend geht es vor allem um:
Staphylococcus aureus-Enterotoxine & Prostaglandin-Rezeptoren
Samter-Trias ist eine Erkrankung, die sich durch bronchiales Asthma, das Vorliegen von nasalen Polypen und eine Unverträglichkeit von Aspirin auszeichnet. Mögliche Gründe sind neben dem gestörten Fettsäurestoffwechsel auch IgE gegen das Staphylococcus aureus-Enterotoxin und Veränderungen bestimmter Prostaglandin-Rezeptoren.
Veränderung des Nasenmikrobioms und Staph. aureus
Staphylococcus aureus (Staph. aureus) ist ein grampositiver Keim, der viele Menschen besiedelt und meist nicht zu einer Erkrankung führt. Hauptsächlicher Übertragungsweg ist die Schmierinfektion oder auch die Verteilung von einem Ort des Befalles (Nasenvorhof, Darm, Vagina) zu einem anderen Ort durch den Keimträger selbst.
Ein großes Problem ist, dass dieser Keim sich besonders gut gegen das Immunsystem schützen kann, z. B. durch die Bildung von Biofilmen, und gegen sehr viele Antibiotika resistent ist. Besonders gefürchtet sind daher die Methicillin-resistenten Staphylokokken, gegen die nur noch sehr spezielle Reserve-Antibiotika wirksam sind.
Staph. aureus-Enterotoxine und TH2-Inflammation bei chronischer Nasennebenhöhlenentzündung mit Polypen
Die chronische Nasennebenhöhlenentzündung mit der Bildung von Polypen, kurz CRSwP, welches englisch für „Chronic Rhinosinusitis with Polyps“ steht, ist ein sehr quälender Symptomkomplex bei Menschen mit einer Intoleranz gegenüber Aspirin. Aspirin gehört zur Gruppe der Nichtsteroidalen Antirheumatika (englisch: NSAID): Daher leitet sich der Name NSAID-Intoleranz ab, weil die Unverträglichkeitsreaktionen auch bei anderen Medikamenten dieser Klasse, wie Ibuprofen und Diclofenac, auftreten.
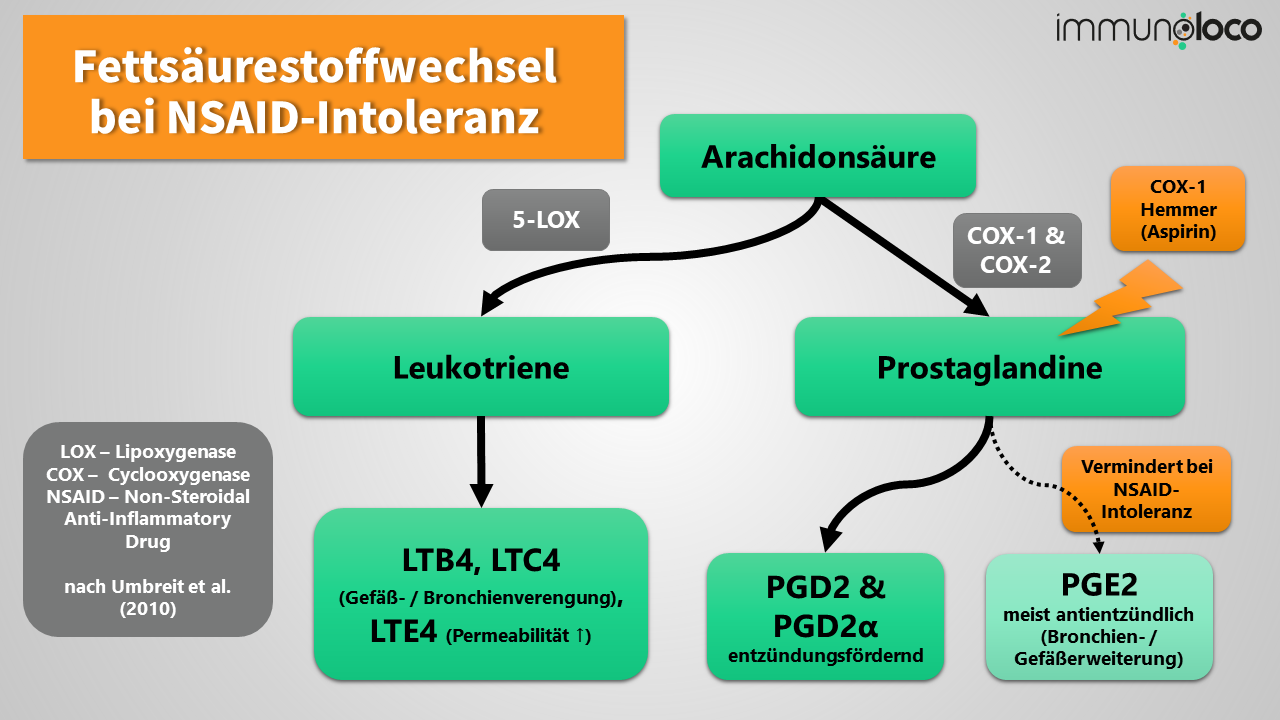
Die Blockade der sogenannten Cyclooxygenasen (kurz: COX) mittels Aspirin oder Ibuprofen verhindern die Produktion entzündungs- und schmerzvermittelnder Botenstoffe aus der Gruppe der Prostaglandine. Dadurch kommt der gewünschte schmerzhemmende, antientzündliche und abschwellende Effekt zustande.
Bei NSAID-Intoleranten kommt es aufgrund der COX-1-Blockade jedoch zu einer vermehrten Synthese von entzündlichen Leukotrienen. Diese sind neben dem Mangel an entzündungshemmenden Prostaglandinen wie PGE2 für die Symptome bei der Samter Trias, wie z. B. Asthma bronchiale, verantwortlich. Auf diesem Blog findet sich ein dedizierter Artikel zum gestörten Fettsäurestoffwechsel, der die Zusammenhänge noch einmal detailliert darstellt.
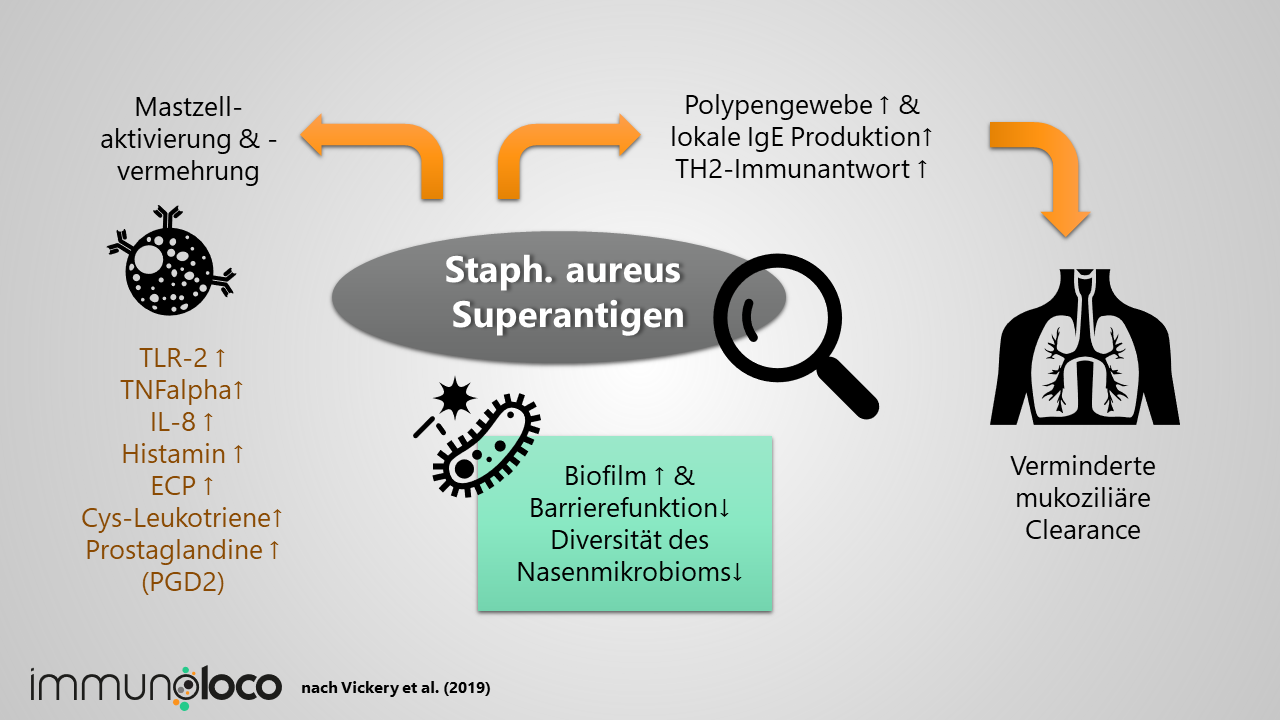
Es hat sich herausgestellt, dass die Polypen bei der NSAID-Intoleranz das Resultat einer verstärkten TH2-Inflammation sind, also einer allergisch-entzündlichen Immunantwort. Diese Immunantwort scheint unter anderem durch die Besiedelung mit Staph. aureus hervorgerufen zu werden, genauer gesagt durch die Produktion von bestimmten Toxinen, sogenannten Enterotoxinen, durch die Bakterien, auf die das Immunsystem dann wieder reagiert.
Das Immunsystem produziert bei besonders schwer Betroffenen häufig Antikörper vom Typ IgE gegen das Staphylococcus aureus-Enterotoxin, sogenannte Staph. aureus-Superantigene: Dadurch kommt es zu einer noch stärkeren Immunreaktion, da weitere Zellen der Immunantwort, vorwiegend B-Zellen, noch mehr aktiviert und angeregt werden, entzündliche Botenstoffe auszuschütten. Am Ende dieser Kaskade stehen bestimmte Interleukine (IL) wie Interleukin-4, IL-5 und IL-13, also Signal-Botenstoffe des Immunsystems, die die IgE-Produktion am Laufen halten und die Freisetzung von Histamin fördern. Zudem kommt es zu einer Vermehrung von Mastzellen.
Die Störung des Nasenmikrobioms und der Schleimhautbarriere
Die Besiedlung mit Staph. aureus scheint dafür zu sorgen, dass die Schleimhautbarriere und die Wundheilung bei Menschen mit CRSwP gestört ist. Dies führen Wissenschaftler auf eine Störung der Wechselwirkung des Nasenmikrobioms mit dem Immunsystem des Wirts zurück. Die Staph. aureus-Stämme fördern anscheinend die entzündliche Immunantwort mit vielen Eosinophilen, die man häufig bei Personen mit Polypen, Asthma und NSAID-Intoleranz findet.
Zudem scheint bei Betroffenen häufiger eine Besiedelung des Nasenvorhofs und der Nebenhöhlen mit Proteobakterien, sowie mit Haemophilus influenzae, vorhanden zu sein. Diese Keime könnten ebenfalls eine Rolle bei der Etablierung der TH2-Inflammation spielen, da sich eventuell auch Superantigene, also IgE, wie bei Staph. aureus, gegen diese Bakterien ausbilden.
Staph. Aureus bekämpfen?
Die Eradikation, also die Entfernung des Staph. aureus, gestaltet sich sehr schwierig. Es wird davon ausgegangen, dass die wiederholten Antibiotikagaben bei Nasennebenhöhlenentzündungen eher dafür sorgen, dass die besonders hartnäckigen Staph. aureus-Stränge, die resistent sind, selektiert werden und damit längerfristig einen größeren Teil des Nasenmikrobioms ausmachen, was das Problem verschärft.
Teilweise zeigen jedoch Antibiotika-Spülungen mit MRSA-wirksamen Antibiosen, wie Mupirocin, eine kurzfristige Verbesserung der Symptome.
Prostaglandin-Rezeptor-Veränderungen bei Samter-Trias-Betroffenen
Neben der TH2-Inflammation, begünstigt durch Staphylococcus aureus-Superantigene, spielt die Störung im Fettsäurestoffwechsel eine große Rolle. Neben der Störung in der Arachidonsäurekaskade und Veränderungen im Prostaglandin E2-Haushalt zeigen sich aber auch Veränderungen auf Prostaglandin E2-Rezeptorebene.
Man kann sich das so vorstellen: Botenstoffe lösen Veränderungen in Zellen und Gewebe aus, indem sie sich an bestimmte Rezeptoren andocken können. Je nach Rezeptor kann der Signalüberträger unterschiedliche Abläufe auslösen. Zudem werden die angestoßenen Prozesse auch darüber beeinflusst, wie viele Rezeptoren, z. B. im Gewebe vorhanden sind. Die Aktivität von PGE2 wird von G-Protein-gekoppelten Membranrezeptoren (GPCRs) vom Subtyp E-Prostanoid (EP) 1–4 bestimmt:
Der EP1-Rezeptor ist eher weniger untersucht, aber ist in Darmzellen und Mastzellen vorhanden. Er beeinflusst die Calcium-Mobilisierung in der Zelle.
EP2 beeinflusst die Bronchienerweiterung und scheint antientzündliche Effekte zu vermitteln.
EP3 erhöht ebenfalls intrazelluläres Calcium und scheint darüber hinaus Pulmonalarterien in der Lunge zusammenziehen zu können. Dieser Rezeptor spielt auch eine Rolle bei der Vermittlung von Schmerzen, Husten und Entzündungen.
EP4 erweitert die Lungenarterien und vermittelt antientzündliche Effekte.
Die Rezeptoren vom Typ EP2 und EP4 sorgen eher für eine Hemmung, fachsprachlich Inhibierung genannt, von Zellfunktionen (über cAMP), während EP1 und EP3 in Zusammenhang gebracht werden mit einer Zellaktivierung (über Calcium-Mobilisierung).
Dieses Zusammenspiel scheint im Gewebe von Menschen mit nasaler Polyposis gestört, z. B. sind in einigen Untersuchungen EP2-Herabregulierungen aufgefallen. PGE2 kann über den EP2-Rezeptor wahrscheinlich die Produktion von Cysteinyl-Leukotrienen von Mastzellen verhindern. Dennoch ist das komplexe Zusammenspiel noch nicht vollständig verstanden.
PGE2 in Aspirin-toleranten versus Aspirin-intoleranten Personen
Bei gesunden NSAID-toleranten Personen wird PGE2 über die Cyclooxygenase-2 (COX-2) hergestellt. Bei Personen mit nasalen Polypen zeigt sich, dass im Gewebe die COX-2-Expression verändert ist, was mit weniger PGE2-Produktion einhergeht.
PGE2 kann die 5-Lipoxygenase (LOX)-Aktivität vermindern und dadurch kommt es zu geringerer Produktion von entzündungsfördernden Leukotrienen. Dies scheint laut einer Untersuchung von Forscherinnen und Forschern aus dem Brigham and Women’s Hospital über die zyklische Adenosinmonophosphat (cAMP) abhängige Proteinkinase A vermittelt zu werden, die teilweise ebenfalls nicht richtig bei Betroffenen funktioniert.
Fazit
All diese Veränderungen im Prostaglandinhaushalt und bei den dazugehörigen Rezeptoren tragen sicherlich zum ausgeprägten Krankheitsgeschehen und zum generellen Entzündungsgeschehen bei. Daneben gibt es Personen, bei denen ein Nasenmikrobiom mit Enterotoxin-produzierenden Staph. aureus eine Rolle spielt, die Entzündungskaskade weiter anzuheizen bzw. am Laufen zu halten.
Ansätze, die eine Homöostase im Nasenmikrobiom und im entzündeten Gewebe mit gestörter Expression der Cyclooxygenasen und Lipoxygenasen schaffen, wären sicherlich in der Therapie sehr hilfreich. Mit monoklonalen Antikörpern, wie Omalizumab oder Dupilumab, kann die TH2-Inflammation eingedämmt werden, aber auch sie schaffen es meist nicht, sämtliche gestörten Stoffwechsel-/Immunmechanismen vollständig zu korrigieren.
Quellen
Staphylococcus aureus | Deutsches Zentrum für Infektionsforschung. Accessed April 24, 2022. https://www.dzif.de/de/glossar/staphylococcus-aureus
Vickery TW, Ramakrishnan VR, Suh JD. The Role of Staphylococcus aureus in Patients with Chronic Sinusitis and Nasal Polyposis. Curr Allergy Asthma Rep. 2019;19(4):21. doi:10.1007/s11882-019-0853-7
Bachert C, Maurer M, Palomares O, Busse WW. What is the contribution of IgE to nasal polyposis? Journal of Allergy and Clinical Immunology. 2021;147(6):1997-2008. doi:10.1016/j.jaci.2021.03.016
Machado-Carvalho L, Roca-Ferrer J, Picado C. Prostaglandin E2 receptors in asthma and in chronic rhinosinusitis/nasal polyps with and without aspirin hypersensitivity. Respir Res. 2014;15:100. doi:10.1186/s12931-014-0100-79
Yoo HS, Shin YS, Liu JN, Kim MA, Park HS. Clinical significance of immunoglobulin E responses to staphylococcal superantigens in patients with aspirin-exacerbated respiratory disease. Int Arch Allergy Immunol. 2013;162(4):340-345. doi:10.1159/000353976
Laidlaw TM, Cutler AJ, Kidder MS, et al. Prostaglandin E2 resistance in granulocytes from patients with aspirin-exacerbated respiratory disease. J Allergy Clin Immunol. 2014;133(6):1692-1701.e3. doi:10.1016/j.jaci.2013.12.1034
Machado-Carvalho L, Roca-Ferrer J, Picado C. Prostaglandin E2 receptors in asthma and in chronic rhinosinusitis/nasal polyps with and without aspirin hypersensitivity. Respir Res. 2014;15:100. doi:10.1186/s12931-014-0100-7


Ältere Kommentare
Diese Kommentare wurden von unserer vorherigen Website übernommen.
Danke Lisa.